
SIE HABEN ODER KENNEN JEMANDEN MIT EINEM VORDEREN KREUZBANDRUPTUR?
Wir fassen auf dieser Seite alle wichtigsten Infos zusammen.
8000 Worte | 50 Minuten Lesezeit
INHALTSVERZEICHNIS
Lieber Kunde, Patient und/oder (Fach)Arzt,
auf dieser Seite möchten wir Ihnen einen umfassenden Einblick in das Thema Vordere Kreuzbandruptur geben. Wir erläutern die Problematik, unser therapeutisches Vorgehen und stellen unsere Behandlungsmethode vor. Grundlage dafür sind wissenschaftliche Erkenntnisse ebenso wie unsere langjährige praktische Erfahrung. Ziel ist es, dass Sie sich bereits im Vorfeld informieren können, um Unsicherheiten zu klären und ein besseres Verständnis für diese Diagnose zu entwickeln.
Die vordere Kreuzbandruptur (VKB-Ruptur) gehört zu den häufigsten Sportverletzungen des Kniegelenks. In Europa erleiden durchschnittlich 81 von 100.000 Einwohnern jährlich eine solche Verletzung. Besonders gefährdet sind Sportarten, die abrupte Brems- und Beschleunigungsmanöver, schnelle Richtungswechsel oder dynamische Landungen nach Sprüngen beinhalten.
Gerade für Sportler spielt die anschließende Rehabilitation eine entscheidende Rolle – nicht nur, um schnellstmöglich und sicher zum Sport zurückzukehren, sondern auch, um das Risiko für eine erneute Ruptur so gering wie möglich zu halten. Wie ein solcher Rehabilitationsprozess aufgebaut ist und welche Faktoren dabei entscheidend sind, erfahren Sie auf dieser Seite.
Wie entsteht die Problematik?
Bei einer vorderen Kreuzbandruptur unterscheidet man grundsätzlich zwischen Verletzungen mit Gegnerkontakt – zum Beispiel in Zweikampfsituationen im Ballsport – und solchen ohne Gegnerkontakt, die häufig durch schnelle Richtungswechsel oder unkontrollierte Landungen entstehen. Der überwiegende Teil der VKB-Risse tritt tatsächlich ohne Fremdeinwirkung auf³.
Typische Bewegungsmuster, die letztlich zum Trauma führen können, sind:
-
Feststehender Unterschenkel kombiniert mit Kniebeugung, Außenrotation des Unterschenkels und gleichzeitiger Innenrotation des Oberschenkels
-
Innenrotation des Unterschenkels bei gleichzeitiger Außenrotation des Oberschenkels
-
Überstreckung (Hyperextension) des Kniegelenks, vor allem bei Landungen auf einem Bein. Ein prominentes Beispiel hierfür ist die Kreuzbandverletzung von Zlatan Ibrahimović im Jahr 2017.



Symptome
Typischerweise treten bei einer vorderen Kreuzbandruptur zwei klinische Merkmale unmittelbar während oder kurz nach dem Verletzungsvorgang auf:
-
Ein deutlich wahrnehmbares „POP“-Gefühl
-
Ein Hämarthros (Blutung ins Gelenk), der meist zu einer raschen Schwellung des Knies führt
In den meisten Fällen sind Kreuzbandrisse sehr schmerzhaft und die Betroffenen bemerken eine schnelle und deutliche Gelenkschwellung. Allerdings kann die Verletzung in seltenen Fällen auch nahezu symptomlos verlaufen.
Die Ausprägung der Symptome hängt stark davon ab, ob Begleitverletzungen wie Meniskus-, Seitenband- oder Kapselschäden vorhanden sind. Sportler berichten in solchen Fällen oft, dass sie nicht mehr auf dem betroffenen Bein auftreten können.
Liegt hingegen eine isolierte Kreuzbandverletzung vor, kann das Bild anders aussehen: Das Knie schmerzt nur mäßig, bleibt relativ beweglich und ist teilweise sogar noch belastbar.
Diagnostik
Die Diagnose einer vorderen Kreuzbandruptur sollte möglichst unmittelbar in den ersten Minuten nach der Verletzung erfolgen. Der Grund: Sobald das Knie anschwillt, wird eine zuverlässige Untersuchung deutlich erschwert.
Klinische Tests
Direkt nach dem Trauma – oder später nach Abklingen der Schwellung – können erfahrene Physiotherapeuten oder spezialisierte Orthopäden verschiedene Funktionstests durchführen:
-
Lachman-Test – gilt in seiner diagnostischen Aussagekraft als gleichwertig mit einem MRT
-
Vordere Schublade
-
Pivot-Shift-Test
-
Lelli’s Test / Lever Sign
Allen Tests ist gemeinsam, dass Ober- oder Unterschenkel fixiert werden, während die andere Komponente gezielt bewegt wird. Die Reaktion des Gelenks wird dabei genau beurteilt und mit der gesunden Gegenseite verglichen.
Ein häufiges Problem bei der Untersuchung: Starke Schmerzen und muskuläre Schutzspannung können die Durchführung und Interpretation der Tests erheblich erschweren.
Bildgebende Verfahren
Wenn die klinische Untersuchung nicht eindeutig möglich ist, kommen bildgebende Verfahren hinzu:
-
MRT (Methode der Wahl)
-
CT (in speziellen Fällen)
Wichtig: Auch hier erschwert eine ausgeprägte Schwellung die Diagnostik. Deshalb sollte die Bildgebung entweder sofort nach dem Trauma oder alternativ in der subakuten Phase (nach Abklingen der Schwellung) erfolgen. Das MRT liefert dabei die besten Informationen über das Kreuzband selbst sowie über mögliche Begleitverletzungen, wie z. B. Meniskus- oder Seitenbandschäden.
Einschränkungen der Bildgebung
Man sollte jedoch im Hinterkopf behalten, dass nicht jede Veränderung, die in der Bildgebung sichtbar ist, auch klinisch relevant sein muss. Manche Auffälligkeiten spiegeln lediglich normale Alterungsprozesse wider – ähnlich wie Falten oder graue Haare an der Oberfläche unseres Körpers.
Anatomie
Das vordere Kreuzband (VKB) liegt im Inneren des Kniegelenks und verbindet – gemeinsam mit dem hinteren Kreuzband – den Oberschenkelknochen (Femur) mit dem Schienbein (Tibia).
Seinen Ursprung hat das VKB in einer kleinen Vertiefung am Oberschenkelknochen. Von dort zieht es schräg nach unten und setzt mittig am Schienbeinplateau an. Das hintere Kreuzband verläuft genau entgegengesetzt – daher auch die Bezeichnung „Kreuzbänder“, da sie sich in der Gelenkmitte überkreuzen.
Wichtig zu wissen: Die genauen Ansatzpunkte des VKB können je nach individueller Anatomie variieren. Gerade dieser Umstand stellt bei einer späteren Operation eine Herausforderung dar, da die korrekte Platzierung des Implantats entscheidend für die Stabilität und Funktion des Knies ist.

Aufgaben der Kreuzbänder
Die Kreuzbänder übernehmen im Knie gleich mehrere entscheidende Funktionen:
Zum einen sorgen sie für Stabilität im Gelenk. Das vordere Kreuzband (VKB) verhindert, dass der Unterschenkel zu weit nach vorne gegenüber dem Oberschenkel rutscht. Das hintere Kreuzband (HKB) übernimmt die Gegenseite und begrenzt den Rückwärtsschub des Unterschenkels. Wichtig ist jedoch: Diese Sicherung ist nicht die Hauptaufgabe der Kreuzbänder. Die eigentliche Stabilität des Knies wird vor allem von der umgebenden Muskulatur getragen – insbesondere von der Oberschenkelvorder- und -rückseite sowie der Wadenmuskulatur. Deshalb spielt eine kräftige und gut koordinierte Muskulatur eine Schlüsselrolle, gerade in der Rehabilitation nach einer Verletzung.
Darüber hinaus erfüllt das VKB eine zweite, ebenso zentrale Funktion: Es liefert eine kontinuierliche Rückmeldung über die auf das Knie wirkenden Kräfte und trägt damit wesentlich zur Tiefensensibilität (Propriozeption) bei. Möglich wird dies durch die Vielzahl an Mechanorezeptoren, die in den Band- und Kapselstrukturen sitzen. Nach einer Verletzung oder Operation ist dieses System deutlich beeinträchtigt – ein gezielter Trainingsfokus auf die Wiederherstellung dieser sensomotorischen Fähigkeiten sollte daher schon früh in der Rehabilitation gesetzt werden. ⁵⁴⁻⁵⁵
Risikofaktoren
Bei der Betrachtung von Risikofaktoren für Kreuzbandverletzungen unterscheidet man zwischen extrinsischen (äußeren) und intrinsischen (inneren) Faktoren.
Extrinsische Faktoren umfassen alles, was von außen auf den Körper einwirkt, zum Beispiel:
-
Die Sportart selbst
-
Genutzte Sportgeräte
-
Fliehkräfte und Bodenreaktionskräfte
-
Gegner oder Hindernisse
Die Verletzungshäufigkeit hängt dabei stark mit dem Kontaktlevel einer Sportart zusammen – je mehr körperlicher Kontakt, desto höher das Risiko. ⁴⁰⁻⁴¹ Besonders riskant sind Bewegungen wie Sprünge, Landungen sowie abruptes Abbremsen oder Beschleunigen. Auch eine ungenügend ausgeprägte Oberschenkel- und Hüftmuskulatur, sowohl in Kraft als auch in Koordination, steigert die Wahrscheinlichkeit eines Kreuzbandrisses.
Intrinsische Faktoren sind dagegen innere, physiologische Voraussetzungen – auf manche davon kann man Einfluss nehmen, auf andere weniger.
Dazu zählen:
-
Körperliche Anatomie⁴
-
Geschlecht und Alter³³
-
Muskelmasse und allgemeine Konstitution
-
Faserverteilung und genetische Faktoren
-
Stoffwechsel und hormonelle Einflüsse
-
Ermüdung und mangelnde Regeneration
-
Ängste oder psychologische Belastungen
-
Neuromuskuläre Leistungsfähigkeit
-
Vorangegangene Kreuzbandverletzungen und die allgemeine Krankheitsgeschichte
Diese Kombination aus äußeren und inneren Faktoren macht deutlich, warum das Risiko für Kreuzbandverletzungen so individuell ist – und warum sowohl Training, Technik als auch Lebensstil einen wichtigen Einfluss haben.
Mythen
„Ohne eine vordere Kreuzband-Rekonstruktion steigt das Arthroserisiko.“
Das Risiko, eine Arthrose zu entwickeln, hängt in erster Linie von Faktoren wie Übergewicht (BMI), körperlicher Inaktivität und einer schwachen Beinmuskulatur ab. ¹⁹
Mehrere wissenschaftliche Studien haben gezeigt, dass Patienten nach einer konservativ behandelten Kreuzbandverletzung nicht häufiger Anzeichen von Arthrose entwickeln als Patienten nach einer Operation. Im Gegenteil – nach einer Operation scheint das Risiko sogar erhöht zu sein, vermutlich aufgrund der wiederholten Entzündungsprozesse, die durch den Eingriff ausgelöst werden. Diese setzen entzündliche Botenstoffe frei, die den Knorpel zusätzlich schädigen können.
Besonders auffällig: Bei der Verwendung einer Patellasehnen-Plastik zeigt sich eine höhere Rate an bildgebend nachweisbarer Arthrose – unabhängig davon, ob die Operation frühzeitig oder erst zu einem späteren Zeitpunkt durchgeführt wurde. ²³⁻²⁸⁻³²⁻⁴⁹
„Ohne eine vordere Kreuzband-Rekonstruktion wird mein Knie nicht mehr ausreichend stabilisiert.“
Die Stabilität eines Gelenks wird immer durch passive und aktive Strukturen gewährleistet.
Im Knie zählen zu den passiven Strukturen die anatomische Form des Gelenks, die Bänder, die Menisken und die Gelenkkapsel. Die wichtigste Rolle übernehmen jedoch die aktiven Strukturen – sprich die Muskulatur des Beines. Sie sorgt im Alltag wie auch im Sport entscheidend für Stabilität.
Das bedeutet: Das vordere Kreuzband allein ist nicht der Garant für ein stabiles Knie. Wenn die Muskulatur gezielt trainiert und auf die jeweilige Belastung vorbereitet wird, kann sie diese Aufgabe übernehmen.
Langzeitstudien, die Patienten nach einer VKB-Rekonstruktion, nach einer Reha mit späterer Operation sowie nach einer konservativen Therapie ohne OP begleitet haben, zeigen ein klares Bild:
Unabhängig von der Behandlungsform konnten keine signifikanten Unterschiede festgestellt werden – weder beim Schmerzempfinden, noch bei Alltags- oder Sportaktivitäten, noch bei der mechanischen Stabilität des Knies oder dem Erreichen des sportlichen Niveaus vor der Verletzung. ⁸⁻²¹⁻²²⁻²³
„Das vordere Kreuzband kann nicht selbst heilen.“
Lange Zeit galt die Annahme, dass ein gerissenes vorderes Kreuzband grundsätzlich nicht zur Heilung fähig ist. Heute wissen wir: Ganz so absolut stimmt das nicht.
Es gibt Studien, die zeigen, dass die Endstümpfe des VKB in bestimmten Fällen wieder aneinanderhaften und verheilen können. Ein Beispiel: In einer Untersuchung wurden 14 sportlich aktive Patienten mit einem akuten Kreuzbandriss beobachtet. Eigentlich war bei allen eine Operation vorgesehen, doch sie lehnten diese ab und entschieden sich stattdessen für eine konservative Behandlung. Bei einer Nachuntersuchung 25–36 Monate nach der Verletzung zeigte sich bei allen Probanden ein vollständig verheiltes vorderes Kreuzband. ¹³
Allerdings muss betont werden: Nicht jede Kreuzbandruptur heilt von allein. Bis heute ist nicht eindeutig geklärt, bei welchen Verletzungsmustern und unter welchen Rahmenbedingungen eine Selbstheilung tatsächlich möglich ist.
Ein spontanes Zusammenwachsen ist möglich, aber nicht die Regel – weshalb die Entscheidung zwischen konservativer und operativer Therapie immer individuell getroffen werden muss.

„Ohne vorderes Kreuzband kann ein Wiedereinstieg in den Sport nicht stattfinden.“
Dieses Vorurteil stimmt so nicht. Mehrere wissenschaftliche Studien zeigen, dass eine Rückkehr zum Sport auch ohne operative Rekonstruktion des VKB möglich ist. ¹⁹˒⁶⁹
Ein Beispiel aus dem Profifußball: 2015 kehrte ein Spieler der englischen Premier League bereits nach nur 8 Wochen konservativer Rehabilitation in den Spielbetrieb zurück – und blieb über 18 Monate hinweg beschwerdefrei. ⁶⁶
Auch im Basketball gibt es eindrucksvolle Belege: DeJuan Blair, ehemaliger NBA-Profi der San Antonio Spurs, spielte mehrere Saisons erfolgreich ohne vordere Kreuzbänder in beiden Knien.
Das zeigt: Ein fehlendes Kreuzband ist nicht automatisch ein Karriereende. Mit strukturierter Rehabilitation, starker Muskulatur und einer sportartspezifischen Vorbereitung ist eine Rückkehr in den Sport durchaus realistisch.
Operation? Ja oder Nein?
Eine der zentralen Fragen nach einer VKB-Verletzung lautet: Muss ich operiert werden oder nicht?
Unsere Antwort: Es kommt darauf an. Ihr behandelnder Orthopäde und Physiotherapeut werden Ihnen Empfehlungen geben – die endgültige Entscheidung liegt jedoch immer bei Ihnen.
Was Sie wissen sollten:
Eine Operation bedeutet eine lange und intensive Reha-Zeit von 9 bis 12 Monaten, in der Sie im Schnitt drei Mal pro Woche Physiotherapie oder Training absolvieren. Das erfordert viel Zeit, Disziplin und Motivation. Wenn Sie dies z. B. wegen Beruf oder Studium nicht leisten können, ist eine konservative Therapie unter Umständen die bessere Wahl.
Ob eine OP sinnvoll ist, hängt in erster Linie von Ihren Alltags- und Sportanforderungen sowie von der erlebten Instabilität ab.
-
In Sportarten mit vielen Drehbewegungen, Landungen und Sprüngen (z. B. Fußball, Rugby, Handball, Volleyball, Hockey) wird meist eine Operation empfohlen.
-
Dennoch zeigen Studien zunehmend, dass operative und konservative Behandlungen in ihren Ergebnissen oft vergleichbar sind.⁸⁻⁹˒²¹˒²²˒²³˒⁴²˒⁴⁴˒⁶⁵˒⁶⁹
Sehr wichtig ist die sogenannte Prä-Rehabilitation (Vorbereitungstraining vor der OP). Studien belegen, dass Patienten, die vor dem Eingriff intensiv trainieren, bessere Ergebnisse erzielen als Patienten, die „nur“ operiert werden.¹⁹˒⁵⁹ Wenn das Knie bereits wieder beweglich ist, keine Schwellung mehr aufweist und Sie auf einem Bein springen können, ist eine präoperative Reha mit Kraft- und Sprungübungen sicher (nur 3,9 % unerwünschte Ereignisse) und bietet Vorteile, die noch Jahre nach der OP messbar sind.¹⁶˒¹⁹
Für Sportarten, die weniger Rotation, Sprünge und Landungen beinhalten – wie Laufen, Radfahren, Schwimmen oder klassisches Fitness-Training – empfehlen wir in vielen Fällen eher eine konservative Therapie.
Operationsarten
Bei einer Kreuzbandplastik wird das gerissene vordere Kreuzband durch körpereigenes Sehnengewebe ersetzt. Der Eingriff erfolgt in den meisten Fällen arthroskopisch (mittels Gelenkspiegelung).
Als Transplantat werden typischerweise verwendet:
-
Teile der Beugesehnen (Semitendinosus-/Gracilis-Sehne),
-
das mittlere Drittel der Patellarsehne (unterhalb der Kniescheibe),
-
oder die Quadrizepssehne (oberhalb der Kniescheibe).
Seltener kommen Allografts (Spendersehnen) oder synthetische Materialien zum Einsatz. Um das neue Kreuzband zu fixieren, werden kleine Bohrkanäle im Ober- und Unterschenkelknochen gesetzt, durch die das Transplantat eingezogen und verankert wird.
Was sagt die Forschung?
Zahlreiche Studien zeigen, dass alle gängigen Transplantate vergleichbare klinische und funktionelle Ergebnisse liefern. Jede Sehne hat jedoch ihre Eigenheiten:
-
Quadrizepssehne: Studien belegen, dass Patienten nach der Entnahme hier deutlich weniger Beschwerden an der Entnahmestelle haben als bei Hamstring-Transplantaten.⁴³
-
Hamstring-Sehne (Kniesehne): Die Entnahme kann die Muskelfunktion der Beuger beeinträchtigen – es kommt häufiger zu reduzierter Kraft und eingeschränkter Propriozeption (also der unbewussten Wahrnehmung von Stellung und Bewegung des Gelenks).³²˒⁶⁸ Dies gilt als relevanter Risikofaktor für spätere Kniearthrose.
-
Patellarsehne: Hier zeigen Studien ein erhöhtes Risiko für Arthrose und Knorpelverlust.¹⁴˒⁴⁹ Zudem verändert sich die Biomechanik, und es können zusätzliche Probleme auftreten:
-
erhöhtes Risiko für Patellafrakturen oder Patellarsehnenrisse,
-
Knieschmerzen beim Knien (bis zu 46 % der Patienten),²³˒²⁸
-
häufig ein anhaltendes Streckdefizit von mehr als 5°.
-
Keine der Methoden ist „perfekt“. Die Wahl des Transplantats hängt von verschiedenen Faktoren ab – etwa Ihrer Anatomie, Ihrem sportlichen Anspruch, Ihrem Beruf und den individuellen Vor- und Nachteilen, die Sie bereit sind in Kauf zu nehmen.

Bohrkanäle

Transplantatdurchzug
Alternative Operationstechnik: Internal Brace
Eine neuere Methode in der Kreuzbandchirurgie ist die sogenannte Internal Brace-Technik. Dabei wird das Kreuzband nicht – wie bei der klassischen Rekonstruktion – ersetzt, sondern erhalten und direkt genäht. Zusätzlich wird eine verstärkende „Brace“ aus einem stabilen Fiber-Tape-Faden eingebracht, die das Kreuzband schützt und unterstützt.
Wann kommt sie infrage?
-
Vor allem bei proximalen (oberflächennahen) Rissen des vorderen Kreuzbands.
-
Der Eingriff sollte innerhalb von vier Wochen nach der Verletzung erfolgen, um optimale Ergebnisse zu erzielen.
Mögliche Vorteile gegenüber der klassischen Rekonstruktion:
-
Kürzere Operationsdauer
-
Kleinere Bohrtunnel, dadurch weniger Eingriff in die Knochenstruktur
-
Keine Entnahmestelle für ein Sehnentransplantat → keine Entnahme-bedingten Beschwerden
-
Erhalt der körpereigenen Propriozeption (Gelenksinn) → potenziell bessere Bewegungs- und Stabilitätsrückmeldung
-
Schnellere Rehabilitation im Vergleich zur klassischen OP
-
Geringere postoperative Muskelkraftdefizite
-
Stabilere Nahtfixierung durch die Verstärkung mit dem Fiber Tape
Einschränkungen:
Die Studienlage ist noch relativ dünn, weshalb diese Methode noch nicht als Standardverfahren gilt und aktuell nur in spezialisierten Kliniken angeboten wird.
Kurz gesagt: Das Internal Brace Verfahren ist ein vielversprechender Ansatz, gerade für Patienten, die von einer schnelleren Regeneration profitieren könnten. Ob es sich langfristig etabliert, hängt jedoch von weiteren Forschungsergebnissen ab.

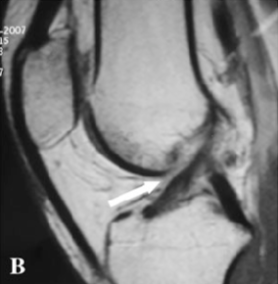
A: Internal Brace Verfahren B: Transplantation
Viel gestellte Fragten
„Muss man nach einer Operation eine Orthese tragen?“
Nach einer Kreuzband-Operation wird häufig eine Orthese für die ersten Wochen empfohlen, um das Transplantat zu stabilisieren und zu schützen.
Allerdings ist die wissenschaftliche Evidenz für diesen Effekt unzureichend.⁴² ⁶⁷
Studien zeigen, dass Hartrahmenorthesen die Aktivität der Beinmuskulatur negativ beeinflussen können – die Muskulatur arbeitet teilweise vermindert oder unkoordiniert verstärkt.¹⁸ ²⁴ ²⁵ Die erhofften funktionellen Effekte wie bessere Tiefensensibilität, Gleichgewicht und Koordination konnten bei Patienten mit Orthesen nicht nachgewiesen werden.² ²⁷ ³⁵ ⁵⁰ ⁶²
Auch eine geringere Rezidivrate (erneute Risse) konnte nicht belegt werden. Das postoperative Ergebnis wird durch eine Orthesen-Versorgung nicht verbessert.²⁷ ³⁵
Die aktuellen Daten sprechen dafür, dass eine Orthese nach Kreuzband-OP keinen klaren Vorteil bringt. Viel wichtiger für die Stabilität des Knies ist ein gezieltes und frühzeitiges Training der Muskulatur.
„Wann kann man wieder mit Joggen anfangen?“
Laufen bildet den Grundstein vieler Bewegungen und ist ein wichtiger Meilenstein im Reha-Verlauf. Es zählt zu den hoch beanspruchenden Anforderungen und erfordert ein gewisses Maß an Kraft sowie neuromuskulärer Kontrolle. Jeder einzelne Schritt beim Laufen erzeugt Bodenreaktionskräfte, die das 2–3-Fache des Körpergewichts erreichen.
Die Entscheidung für den Laufbeginn wird nicht zeitbasiert, sondern kriterienbasiert getroffen. Durchschnittlich erfolgt der Einstieg zwischen der 8. und 16. Woche.⁶ ⁷
Kriterien für den Beginn des Laufbandtrainings bei 8 km/h:
-
Schmerz auf einer Skala von 0–10 bei < 2
-
Keine Schwellung, kein Erguss mehr vorhanden
-
Volle Extension/Streckung des Beins möglich
-
95 % der Knieflexion/Beugung im Vergleich zur nicht betroffenen Seite
-
Isometrische Kraftentwicklung der Kniebeuger und -strecker von mindestens 70 % im Vergleich zur nicht betroffenen Seite
-
Funktionelle Tests (z. B. Step-Ups, Einbein-Sprünge, Einbein-Squats) gut durchführbar; hierbei sollten mindestens 70 % der Leistung der nicht betroffenen Seite erreicht werden
„Wann kann ich zum Sport / Wettbewerb zurückkehren?“
Die durchschnittliche Rückkehr zum Sport erfolgt nach etwa 6 Monaten, zum Wettbewerb nach ungefähr 8 Monaten. Innerhalb der ersten 24 Monate nach einer Verletzung ist das Risiko einer erneuten Ruptur jedoch besonders erhöht.
Auch wenn die biologische Reifung und Reorganisation des neuen Implantats zu diesem Zeitpunkt noch nicht vollständig abgeschlossen ist, kann bei vollständigem Erreichen der notwendigen RTC-Kriterien die Sportfreigabe erteilt werden.
Was können Sie als Patient oder Arzt bei/von uns erwarten?
Zu Beginn der ersten Therapiesitzung erwartet Sie – wie bei jedem unserer neuen Patienten – ein ausführliches Anamnesegespräch mit einem unserer Therapeuten. Dabei erfassen wir alle für die Therapie relevanten Informationen und schließen mögliche Kontraindikationen oder sogenannte „Red Flags“ aus. Anschließend folgt eine gründliche Untersuchung, um den aktuellen Rehabilitationsstatus präzise festzulegen.
Gemeinsam mit Ihnen erstellen wir danach ein individuelles Anforderungsprofil, das exakt auf Ihre Sportart oder die täglichen Anforderungen Ihres Alltags abgestimmt ist. Ziel ist es, einen klar definierten IST-Zustand zu bestimmen und einen realistischen Soll-Zustand zu formulieren. Dieser Prozess wird kontinuierlich durch die Therapie begleitet, regelmäßig überprüft und angepasst, sodass jederzeit ein aktuelles Bild Ihres Leistungsniveaus vorliegt.
Um das volle Potenzial der Behandlung auszuschöpfen, bieten wir Ihnen optional die Möglichkeit einer erweiterten Therapiezeit an. Diese Zusatzleistung gewährleistet eine noch intensivere Betreuung, höchste Qualität in der Therapie und ein optimales Ergebnis.
Nach einer detaillierten Analyse Ihrer Sportart oder Alltagsbelastung erstellen wir auf Basis aller gesammelten Informationen einen maßgeschneiderten Rehabilitationsplan. Dieses Reha-Modell ist ein dynamisches, sich ständig neu bewertendes System: Es orientiert sich nicht an festen Zeitvorgaben, sondern an klar definierten Kriterien und berücksichtigt dabei stets den aktuellen Wundheilungsprozess sowie den individuellen Leistungsstand.
Kriterienbasierte vs. zeitbasierte Rehabilitation
Grundsätzlich sind Rehabilitationspläne nichts Schlechtes. Sie geben eine hilfreiche Übersicht über den groben Verlauf der Genesung. Allerdings bringt ein rein zeitbasierter Ansatz auch einige Nachteile mit sich, die wir Ihnen im Folgenden näher erläutern möchten:
Zeitbasiertes Voranschreiten:
-
Orientiert sich hauptsächlich an der Zeit nach der Verletzung oder Operation, ohne die tatsächliche Dauer des gesamten Rehabilitationsprozesses zu berücksichtigen. Dieser dauert meist deutlich länger, als zeitbasierte Pläne vorsehen.
-
Stützt sich auf „Lehrbuch-Heilungszeiten“, die jedoch von Patient zu Patient stark variieren. Faktoren wie körperliche Verfassung, Übergewicht, Trainingszustand, Motivation, Nebenerkrankungen oder die Immunfunktion spielen hier eine entscheidende Rolle.
-
Auch externe Einflüsse wie Stress, Ernährung, Schlafqualität und Lebensstil wirken sich auf die Wundheilung aus.
-
Jeder Patient erhält im Prinzip den gleichen Plan – individuelle Unterschiede und Bedürfnisse werden zu wenig berücksichtigt.
Kriterienbasiertes Voranschreiten:
-
Der Fortschritt erfolgt erst nach dem Erreichen klar definierter Meilensteine, wobei natürliche Heilungszeiten selbstverständlich respektiert werden – denn schneller als biologisch möglich geht es nicht.
-
Der aktuelle Leistungsstand wird regelmäßig überprüft und messbar gemacht. Dadurch können Schwachpunkte frühzeitig erkannt und gezielt behoben werden, was gleichzeitig eine wichtige präventive Wirkung hat.
-
Unterschiedliche Verletzungen und Beschwerdebilder erfordern unterschiedliche Programme. Die kriterienbasierte Rehabilitation lässt sich flexibel anpassen und sorgt für ein engmaschiges Monitoring des individuellen Heilungsverlaufs.
Eine rein zeitbasierte Reha ist aus heutiger Sicht nicht mehr zeitgemäß. Sie berücksichtigt zu viele individuelle Faktoren nicht und sieht den Patienten nicht als das, was er ist – ein Individuum mit einzigartigen Voraussetzungen. Die kriterienbasierte Rehabilitation bietet hier einen deutlich moderneren, individuelleren und erfolgreicheren Ansatz.

Ligamentisierung des Implantats
Bei einer Kreuzband-Transplantation zeigen Untersuchungen am Mensch und Tier, dass die neu eingesetzten Sehnentransplantate einen komplexen biologischen Umbauprozess durchlaufen. Dieser Prozess wird als „Ligamentisierung“ bezeichnet. Gemeint ist damit die Umwandlung der ursprünglich als Sehne entnommenen Struktur in ein bandähnliches Gewebe. Das Transplantat bleibt während des gesamten Verlaufs lebensfähig, durchläuft jedoch mehrere Phasen mit unterschiedlichen biologischen Eigenschaften.
Histologisch wird der Heilungsverlauf in drei Hauptphasen unterteilt¹¹:
-
Frühe Heilungsphase
-
In dieser Phase kommt es im zentralen Anteil des Transplantats zu einer Nekrose (Zelluntergang).
-
Als Ursache gilt der Kontakt mit der Gelenkschmiere, wodurch Prozesse angestoßen werden können, die den Heilungsverlauf beeinträchtigen¹.
-
Die Stabilität des Transplantats ist in dieser Phase besonders gefährdet.
-
-
Proliferationsphase
-
Entscheidend ist hier das Einwachsen neuer Blutgefäße in das Transplantat.
-
Nur durch eine ausreichende Gefäßversorgung kann Sauerstoff transportiert und eine Zellneubildung ermöglicht werden.
-
Eine unzureichende Gefäßversorgung kann zu Sauerstoffmangel führen und die Heilung erheblich beeinträchtigen³⁸ ⁴³.
-
-
Maturationsphase
-
In dieser letzten Phase reift das Gewebe zunehmend zu einer bandähnlichen Struktur heran.
-
Eine Anpassung des VKB-Implantats an die Eigenschaften des ursprünglichen VKB kann frühestens nach etwa 2 Jahren beobachtet werden⁴⁸ ⁷⁰.
-
Trotz dieser Anpassung bleiben Unterschiede in der Verteilung und Organisation der kollagenen Bindegewebsfasern bestehen.
-
Wichtige Einflussfaktoren:
-
Der Einsatz von NSAR (z. B. Ibuprofen, Diclofenac) oder COX-2-Hemmern direkt nach der Operation sollte kritisch hinterfragt werden. Studien zeigen, dass diese Medikamente das ohnehin geschwächte Transplantat zusätzlich negativ beeinflussen können⁶⁰.
-
Alkohol- und Nikotinkonsum wirken sich ebenfalls stark negativ auf die Gefäßneubildung und damit auf die Transplantatgesundheit aus. Ein Verzicht auf beide Faktoren ist für ein optimales Therapieergebnis entscheidend.
